细菌死活染色试剂盒(DMAO/PI)
| 英文名 | DMAO/PI Live/Dead Bacterial Double Stain Kit | ||
| 产品编号 | FS4006 | ||
| 产品分类 | 微生物培养基 | ||
| 纯度 | N/A | 储存条件 | -20℃ |
产品简介
DMAO,即N, N-dimethylaniline N-oxide,是一种核酸绿色荧光染料,对于革兰氏阳性和阴性细菌均适用,且既能染色活细菌,也能染色死细菌。该染料具有膜通透性,能透过细胞膜,优先结合双链DNA。DMAO非常稳定,在室温下进行常规操作和保存不易降解。PI是一种非渗透性荧光染料,不能穿过具有生物活性的细胞质膜,因此对于具有完整细胞膜的细菌不能染色。而对于坏死细菌,其细胞膜的完整性丧失,PI可进入细胞核并与双链DNA结合,并嵌入细菌的DNA双螺旋形成PI-DNA复合物从而产生红色荧光,这种结合很少或几乎没有序列偏好,每4-5个碱基对插入一分子PI染料。将DMAO与PI联合使用检测细菌的死活,具有完整细胞膜的活细菌呈现绿色荧光,细胞膜受损的死细菌同时呈现绿色与红色荧光。
DMAO-DNA复合物的最大激发光波长为503nm,最大发射光波长为530nm;PI-DNA复合物的最大激发光波长为535nm,最大发射光波长为617nm。DMAO-DNA和PI-DNA的激发光谱和发射光谱参考图1,可分别使用FITC和Cy3通道观察。
本品中文名称细菌死活染色试剂盒(DMAO/PI),英文名称LIVE/DEAD Bacterial Staining Kit with DMAO & PI,或LIVE/DEAD Bacterial Viability Kit with DMAO and PI,也称细菌活力检测试剂盒(Bacterial Viability Assay Kit)或细菌毒性检测试剂盒(Bacterial Cytotoxicity Assay Kit),是一种高效、便捷、灵敏的基于DNA绿色荧光染料DMAO和红色荧光染料碘化丙啶(Propidium iodide, PI)的双荧光染色法检测细菌死活的试剂盒。本试剂盒检测时,活细菌呈现绿色荧光,死细菌呈现绿色和红色两种荧光。本试剂盒可使用荧光显微镜、激光共聚焦显微镜、荧光酶标仪、流式细胞仪等荧光检测系统进行检测。
本试剂盒提供的DMAO与PI均为1000×的储存液,溶液经过优化,对大多数细菌都适用,但为了获得更满意的结果,对于不同类型的细菌请自行进行一定的浓度摸索,DMAO和PI的使用终浓度一般为0.5-2×,最优先的推荐终浓度为1×。同时,本试剂盒提供检测缓冲液,该缓冲液可用于细菌死活染色工作液的配制。
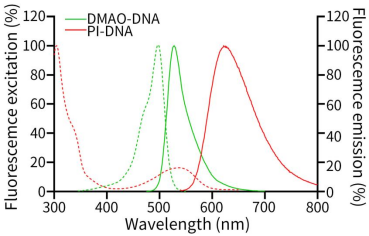
图1.DMAO-DNA和PI-DNA的激发光谱和发射光谱。
产品组成
|
编号 组分 |
FS4006-活细菌/死细菌双染试剂盒(DMAO/PI) (DMAO /PI Live/Dead Bacterial Double Stain Kit) |
规格 |
规格 |
规格 |
保存方法 |
|
200T |
500T |
1000T |
|||
|
FS4006-A |
DMAO Solution (1000×) |
20μl |
50ul |
100ul |
-20ºC避光 |
|
FS4006-B |
PI Solution(1000×) |
20μl |
50ul |
100ul |
-20ºC避光 |
|
FS4006-C |
检测缓冲液 |
1ml |
5ml |
10ml |
-20ºC保存 |
保存与运输方法:-20℃避光保存,有效期一年。 冰袋运输。
使用方法(以下步骤仅用作示例以指导科研人员开展自身细菌样本的染色。)
一、培养条件和细菌悬液的制备
【注意】:用本试剂盒进行细菌染色,务必要小心去除培养基残留,因为,核酸和其它培养基成分可能以不可预料的方式与DMAO和PI结合,导致染色结果发生不可接受的变动。简单的一次清洗步骤通常足以去除培养基内含的培养基成分干扰物残留。不建议使用磷酸盐清洗缓冲液,因此可能降低染色效率。
1.1 用营养肉汤培养大肠杆菌或金黄色葡萄球菌(30ml)使其生长至对数生长后期。
1.2 于10000×g离心10-15min,浓缩25ml细菌培养物。
1.3 吸走上清液,用2ml 0.85% NaCl或适当缓冲液来重悬沉淀。
1.4 取1ml重悬菌液分别加入含20ml 0.85% NaCl或适当缓冲液的30-40ml离心管(设置为活细菌组),用含20ml 70%异丙醇(也可以用其他方法比如高热处理杀死细菌)的30-40ml离心管(设置为死细菌组)。
1.5 两管样品(分别为活细菌组和死细菌组)于室温孵育1h,每隔15min颠倒混匀一次。
1.6 两管样品(分别为活细菌组和死细菌组)于10000×g离心10-15min。
1.7 用20ml 0.85% NaCl或适当缓冲液重悬沉淀,并且按照步骤1.6再离心一次。
1.8 分别用10ml 0.85% NaCl或适当缓冲液重悬两管样品。
1.9 分别取3ml菌液测定670nm的光密度(OD670),用玻璃或丙烯酸酯比色皿(1cm路径)。
1.10 对于大肠杆菌或金黄色葡萄球菌的建议染色浓度,根据你的仪器类型(荧光显微镜、荧光光度经、荧光酶标仪)或流式细胞仪来参考相应部分的染色条件。
二、荧光显微镜操作步骤
2.1活菌和死菌的荧光可能用标准的荧光素长通滤片设置来同时观察。替代方案的话,活菌(绿色荧光)和死菌(红色荧光)可分别用双通道:荧光素FITC和Texas Red带通滤光片设置。用于本试剂盒检测的建议荧光显微镜滤片设置见表1。
表1 适用于本试剂盒检测用的常见滤光片特征
|
Omega滤光片* |
Chroma滤光片* |
注意事项 |
|
XF25, XF26, XF115 |
11001, 41012, 71010 |
用于同时观察DMAO和PI染色的长通和双发射滤光片 |
|
XF22, XF23 |
31001, 41001 |
仅用于观察DMAO的带通滤光片 |
|
XF32, XF43, XF102, XF108 |
31002, 31004, 41002, 4100 |
仅用于观察PI的带通滤光片 |
|
用于荧光显微镜观察的推荐带通滤光片。Omega滤光片由Omega Optical提供,Chroma滤光片由Chroma Technolog公司提供。 |
||
油镜100×计数>5个视野,计算存活率:存活率(%)=绿色荧光细胞数/(绿色+红色光细胞数)×100
三、流式细胞仪操作步骤
仪器的检测配置可能要因实际情况来调整,但此处列出的检测技术和设置参数适用于市场上绝大多数流式细胞仪。
FL1通道: (530/30nm) DMAO (检测活菌)
FL3通道: (>670nm) PI (检测死菌)
阈值设定:排除粒径<0.2um碎片(避免假阳性)
结果判断与数据验证分析
|
表型
|
DMAO信号 |
PI信号 |
生理状态判定 |
|
健康活菌 |
+++ |
- |
代谢活跃,膜完整 |
|
早期凋亡菌 |
++ |
+ |
膜轻微损伤,酶活性存留 |
|
死菌 |
- |
+++ |
膜崩解,DNA暴露 |
|
VBNC(活不可培) |
+ |
- |
休眠态,需结合ATP检测确认 |
注意事项
1) 由于试剂盒内DMAO和PI的组分量少,室温回温充分融化后,务必低速离心沉至管底后再开盖。
2) 两款探针溶液本身就是溶于DMSO中,所以后续无需再单独添加,第一次使用可将DMAO和PI根据单次用量分装保存,密封后置于≤-20℃避光保存。
3) 组分C检测缓冲液经过过滤除菌处理,在使用时须注意避免微生物污染,否则很可能严重影响染色效果。如果检测缓冲液发生浑浊等明显的微生物污染,就不能继续使用。
4) DMAO 和PI结合核酸,PI是潜在的诱变剂,目前没有数据阐明DMAO的诱变性或毒性,两种试剂使用都需做恰当防护。DMSO能促进有机分子进入组织。强烈建议处理DMSO储存液时戴双层手套。对于核酸染料,含此类染料的试剂经活性炭吸附后再进行废液处理。活性炭之后经焚烧来破坏染料。
5) 为了您的安全和健康,请穿实验服并戴一次性手套操作。
常见问题及解决方案
|
问题现象 |
原因分析 |
优化解决方案 |
|
背景荧光高 |
染料残留或菌体自荧光 |
增加缓冲液洗涤次数(≥3次),增加0.1%BSA阻断 |
|
革兰氏阳性菌染色弱 |
细胞壁阻挡PI渗透 |
预冷甲醇固定5 min或使用通透增强剂0.1%Triton X-100 |
|
荧光信号淬灭快 |
光照过度或氧化损伤 |
|
|
假阳性死菌 |
离心力过大导致机械损伤 |
离心力降至5000g以下,改用滤膜浓缩法 |
相关产品
|
货号 |
名称 |
规格 |
|
20µl |
||
|
50µl |
||
|
10mg |
||
|
10mg |
||
|
5mg |
||
|
Live/Dead Bacterial Double Stain Kit 活细菌/死细菌双染试剂盒(SYTO 9/PI ) |
40T |
|
|
200T |


.jpg)
