Lipid Peroxidation Assay Kit with BODIPY 581/591 C11脂质过氧化检测试剂盒(BDPY 581/591 C11)
| 英文名 | Lipid Peroxidation Assay Kit with BODIPY 581/591 C11 | ||
| 产品编号 | FS1460 | ||
| 产品分类 | 荧光探针及染色 | ||
| 纯度 | N/A | 储存条件 | -20ºC |
产品简介
脂质过氧化(Lipid peroxidation, LPO)是许多病理状态的关键变化,会导致一些重要的膜蛋白结构和功能的改变,甚至导致细胞功能障碍和广泛的细胞和组织损伤,和许多疾病的发生密切相关。广泛的脂质过氧化是铁死亡的关键下游特征。铁死亡(Ferroptosis)是一种铁依赖性、与细胞凋亡不同的细胞死亡形式。在二价铁的作用下,细胞抗氧化能力减弱,细胞膜或细胞器膜上含不饱和脂肪酸长链的磷脂分子被过氧化而破坏, 造成细胞膜破裂,从而导致调节性细胞死亡(Regulated cell death, RCD),也称程序性细胞死亡(Programmed Cell Death, PCD) [1-3]。
BDPY 581/591 C11 (也称BODIPY 581/591 C11)即为其中一种。BDPY 581/591 C11的分子式为C30H35BF2N2O2,分子量为504.42,CAS号为217075-36-0,也称脂质过氧化传感器(Lipid Peroxidation Sensor)、脂质过氧化探针(Lipid Peroxidation Probe)、BDPY 581/591十一烷酸,具有良好的光稳定性、低荧光伪影特质,可以快速入膜,是一种用于检测活细胞内脂质过氧化及抗氧化能力的荧光探针。其还原态和氧化态,均具有良好的亲脂性,二者处在磷脂双分子层的两个不同区域,均不会自发离开细胞膜磷脂双分子层。BDPY 581/591 C11对各种氧自由基以及过氧亚硝酸盐灵敏,但对超氧化物、一氧化氮、过渡铁离子和氢过氧化物不灵敏[4-6]。
BDPY 581/591 C11的还原态产物最大激发波长为581nm,最大发射波长为591nm,主要为红色荧光,此时红绿荧光比值较大;经脂质过氧化氢物氧化后,激发和发射波长最大值偏移至约488/510nm,主要为绿色荧光,此时红绿荧光比值降低。实际观察时,使用常规的观察红色荧光和绿色荧光的设置即可,并可通过红绿荧光的比值确定脂质过氧化的程度。
本试剂盒脂质过氧化检测试剂盒(BDPY 581/591 C11) (Lipid Peroxidation Assay Kit with BDPY 581/591 C11或Lipid Peroxidation Assay Kit with BODIPY 581/591 C11)是一种以BDPY 581/591 C11 (也称BODIPY 581/591 C11)为荧光探针,快速高灵敏地检测细胞内脂质过氧化程度变化的试剂盒。本试剂盒可使用荧光显微镜、激光共聚焦显微镜、荧光酶标仪、流式细胞仪等荧光检测系统进行检测。试剂盒提供的BDPY 581/591 C11为2mM储存液。该溶液经过优化,对大多数细胞都适用,但为了得到更满意的结果,对于不同类型的细胞请自行进行一定摸索,BDPY 581/591 C11的终浓度一般为2-10μM,最优先的推荐终浓度为2μM。该探针比较灵敏,使用较低浓度就能检测到相应的特异性结果。同时,本试剂盒提供的Lipid P作为诱导细胞内脂质过氧化物生成的阳性对照,终浓度通常为0.5-2X,最优先的推荐终浓度为1X。使用本试剂盒检测细胞内脂质过氧化的效果参考图1。
产品组成
|
名称 编 号 |
FS1460 (100~1000次) |
FS1460 (500~5000次) |
Storage |
|
试剂A: BDPY 581/591 C11(2mM) |
100ul |
500ul |
-20℃避光 |
|
试剂B:Lipid P (1000X) |
20µl |
100ul |
-20℃ |
|
使用说明书 |
1份 |
||
储存条件:-20℃避光保存,1年有效。小量分装避免反复冻融,-80ºC可保存更长时间。
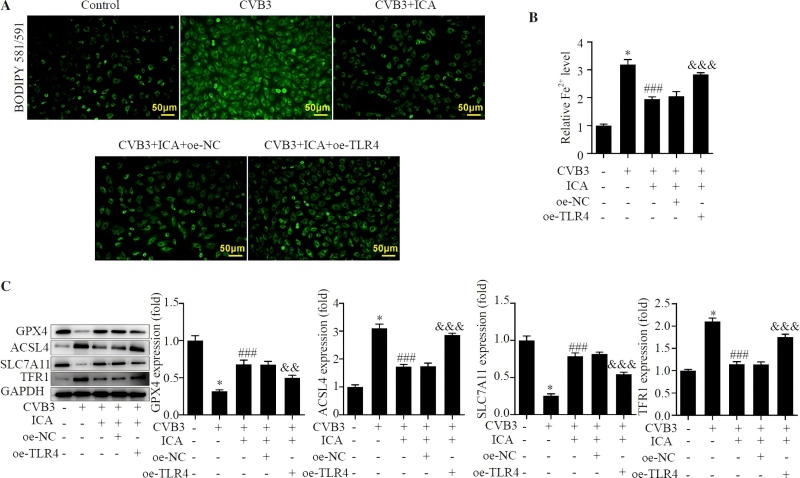
图1.:ICA通过调节TLR4对CVB3诱导的铁死亡的影响。(A)TLR4过表达后细胞内脂质过氧化的水平。(B)TLR4过表达对使用铁比色法试剂盒测定的细胞内铁水平的影响。(C)TLR4过表达对采用Western blotting法测定的铁死亡相关蛋白水平的影响。*P<0.001与对照组相比;### P<0.0001与CVB3组相比;&& p<0.01,&&&p<0.001与CVB3+ICA+oe-NC组相比。(来源文献:Icariin ameliorates viral myocarditis by inhibiting TLR4-mediated ferroptosis-Asian Pacific Journal of Tropical Biomedicine 14(3):p 106-114, March 2024).
本试剂盒小包装和中包装,BDPY 581/591 C11 (2mM)按照1:1000的比例稀释,6孔板每孔检测体系为1ml时,可以分别进行100和500次检测;96孔板每孔检测体系为100μl时,可以分别进行1000和5000次检测。
使用方法(以下步骤仅做参考,具体请根据实际情况或参考文献资料来调整。)
1. 探针BDPY 581/591 C11染色工作液的配制。
(1)建议收到产品后,根据单次使用量,对母液进行小量分装,每次使用一管,试剂-20℃避光冻存,一年稳定。
(2) 开始实验前,使用 HBSS 缓冲液或 PBS 稀释储存液到需要的工作浓度。工作浓度为根据不同细胞的预实验结果确定的最佳工作浓度,一般染色终浓度 500-1000 倍稀释。1000 倍稀释适合大多数细胞样本的检测。
(3) 首次使用建议优化探针浓度,选择荧光信号强且细胞活力无显著下降的浓度。
(4) 为了降低过度加载染料导致的潜在背景和细胞毒性,在不影响实验结果的前提下应尽可能低浓度染色。另外,浓度过高也可能造成非特异性染色。
(5) 不可以使用含血清培养基稀释探针。
(6) 工作液现配现用。
(7) 以下步骤使用的探针为此步骤配置好的探针工作液。
6孔细胞培养板为例:每孔所需BDPY 581/591 C11染色工作液的量为1ml,其它培养器皿的BDPY 581/591 C11染色工作液的用量以此类推;对于细胞悬液每50-100万细胞需0.5ml BDPY 581/591 C11染色工作液。取适量BDPY 581/591 C11 (2mM),按照每1µl BDPY 581/591 C11 (2mM)加1ml 1×PBS/HBSS细胞培养级 (CAT#FSH055/FSH041)的比例稀释BDPY 581/591 C11,混匀后即为BDPY 581/591 C11染色工作液(2μM)。
【注】:配制BDPY 581/591 C11染色工作液时注意避光,且须现配现用,不宜保存后使用。
【注】:BDPY 581/591 C11染色工作液中BDPY 581/591 C11的最终浓度需根据不同细胞系和实验体系通过预实验进行优化。BDPY 581/591 C11的推荐工作浓度为2μM,可以在2-10μM范围内摸索最佳工作浓度。
2.阳性对照的设置。
把试剂盒中提供的Lipid P (1000X)推荐按照1:1000的比例加入到细胞培养液中,处理细胞4小时。随后按照步骤3加入BDPY 581/591 C11染色工作液,进行细胞内脂质过氧化产物的检测。对于大多数细胞,通常Lipid P (1X)处理4小时后脂质过氧化产物含量大量增加,BDPY 581/591 C11染色后观察应呈较强的绿色荧光,红色荧光减弱;而正常的细胞经BDPY 581/591 C11染色后应显示较强的红色荧光,绿色荧光较弱。对于特定的细胞,Lipid P作用浓度和作用时间可能有所不同,需自行摸索最佳工作浓度作用时间,甚至某些细胞可能对Lipid P不敏感。
3.对于悬浮细胞。
a.细胞按照实验设计进行一定处理后,计数。取适当细胞600×g室温离心5分钟,弃上清,加入适当体积的BDPY 581/591 C11染色工作液重悬细胞,使细胞密度为100-1000万/ml。
b.细胞培养箱中37ºC孵育10-30分钟,不同的细胞最佳孵育时间不同。以20分钟作为初始孵育时间,根据作用细胞对孵育时间进行适当优化以得到最佳的效果。
c.37ºC孵育结束后,600×g 4ºC离心3-4分钟,沉淀细胞。弃上清,注意尽量不要吸除细胞。
d.用PBS洗涤2次:加入1ml PBS重悬细胞,600×g 4ºC离心3-4分钟,沉淀细胞,弃上清。再加入1ml PBS重悬细胞,600×g 4ºC离心3-4分钟,沉淀细胞,弃上清。
e.再用适量PBS重悬细胞后,用荧光显微镜或激光共聚焦显微镜观察,也可以用荧光分光光度计检测或流式细胞仪分析。
4.对于贴壁细胞。
【注】:对于贴壁细胞,如果希望采用流式细胞仪检测,可以先消化并收集细胞,重悬后参考悬浮细胞的检测方法。
a.对于6孔板的一个孔,吸除培养液,根据具体实验如有必要可以用PBS或其它适当溶液洗涤细胞一次。如果使用其它的多孔板,各种试剂的用量需要相应按比例调整。
b.加入1ml BDPY 581/591 C11染色工作液。细胞培养箱中37ºC孵育10-30分钟,不同的细胞最佳孵育时间不同。以10分钟作为初始孵育时间,根据作用细胞对孵育时间进行适当优化以得到最佳的效果。
c.37ºC孵育结束后,吸除上清,用PBS洗涤2次。
d.加入2ml PBS,荧光显微镜或激光共聚焦显微镜下观察。如果考虑使用荧光酶标仪检测,推荐使用全黑96孔细胞培养板或黑色透明底96孔细胞培养板,分别进行顶读或底读模式进行荧光检测。
5.参数设置。
BDPY 581/591 C11的还原态产物最大激发和发射波长为581/591nm,荧光参数设置参考碘化丙啶或Cy3;经脂质过氧化氢物氧化后,激发和发射波长最大值偏移至约488/510nm,荧光参数设置参考GFP或FITC。还原态时主要为红色荧光,此时红绿荧光比值较大,氧化态主要为绿色荧光,此时红绿荧光比值降低,可通过红绿荧光的比值确定脂质过氧化的程度。
结果示例(仅供参考):
|
样品 |
平均比值(F 绿/ F 红) |
相对脂质过氧化水平 |
模型 |
|
空白对照 |
0.23 |
1.00 |
仅加无血清培养基,不加探针和诱导剂 |
|
阴性对照 |
0.25 |
1.09 |
细胞+铁死亡抑制剂预处理1小时,再按后续步骤孵育探针 |
|
阳性对照 |
1.87 |
8.13 |
细胞+Lipid P (1X)处理4小时,再孵育探针 |
|
实验组(药物) |
1.24 |
5.39 |
细胞+待检测药物处理,培养特定时间后孵育探针。 |
注意事项
1) 正式实验前请选取几个样本做预实验,以优化实验条件,取得最佳实验效果。
2) 螺旋盖微量试剂管装的试剂在开盖前请短暂离心,将盖和管内壁上的液体离心至管底,避免开盖时试剂损失。
3)荧光染料均存在淬灭问题,请尽量注意避光,以减缓荧光淬灭。
4)为了您的安全和健康,请穿实验服并戴一次性手套操作。
常见问题分析Q&A:
Q1:脂质过氧化物结果如何分析?
A1:由于荧光强度容易波动,单独使用绿色或红色荧光强度进行分析可能不稳定。因此,推荐使用绿色与红色荧光的比值(Green/Red Ratio)来量化脂质过氧化水平,这种比率型分析能有效减少因染料加载量、细胞数量差异等带来的误差。
Q2:荧光照片效果不好?
A2:荧光拍照存在很多变量,每一个变量都会严重影响拍照效果。荧光拍摄条件:拍摄环境、显微镜品牌和激发荧光决定了镜下观察的效果。同样的操作方法和切片,在不同品牌显微镜下显示出完全不同的荧光强度。荧光衰减:荧光物质的衰减通常都是非常明显的。同样的一组切片,1小时内拍摄和8小时后拍摄,荧光效果完全不同。最好用激光共聚焦显微镜,激光共聚焦显微镜的分辨率比普通荧光显微镜要高的多,通常同一张片子激光共聚焦的效果明显更优。
Q3:背景荧光比较高?
A3:在没有细胞外酯酶和其他氧化酶的情况下,荧光随时间的逐渐增加可能是来自自发水解,导致水解的原因可能与大气氧化或光诱导氧化有关。
Q4:荧光强度在变化?
A4:可以观察到荧光的逐渐增加(由于自动氧化)或减少(由于细胞中的染料损失或光漂白)。在没有任何刺激或诱导的情况下,健康的未经处理的细胞中的荧光突发可以指示细胞死亡或一些其他氧化事件的进展。注意检测时平行操作即可。
常见问题及解决方案:
|
问题 |
可能原因 |
解决方案 |
|
无绿色荧光信号 |
氧化诱导不足 |
验证阳性对照 |
|
背景荧光过高 |
探针未充分洗涤 |
增加洗涤次数,使用无血清培养基加载 |
|
红色信号过弱 |
探针浓度过低或过度氧化 |
优化探针浓度,缩短孵育时间 |
|
结果不可重复 |
光氧化或操作差异 |
全程避光,严格标准化孵育时间和温度 |
相关产品
|
产品货号 |
产品名称 |
规格 |
|
FS1359 |
BODIPY 558/568 C12 脂质转运荧光探针 |
1mg |
|
FS1360 |
C11 BODIPY 581/591 脂质过氧化荧光探针 |
1mg |
|
FS1176 |
H2DCFDA (DCFH-DA) 活性氧(ROS)荧光探针 |
10mg |
|
FS1176S |
活性氧(ROS)检测试剂盒 |
100~500T |
|
FS1399 |
CM-H2DCFDA活性氧荧光探针/ROS荧光探针 |
50ug |

.jpg)
